ASCO重磅速遞丨李進(jìn)教授:里程碑成就!DCR 95.5%,PFS 6.9個月,呋喹替尼聯(lián)合信迪利單抗開啟晚期CRC治療新篇章
作為一款我國自主原研的抗血管內(nèi)皮細(xì)胞生長因子受體(VEGFR)小分子酪氨酸激酶抑制劑(TKI),呋喹替尼獲得國家藥品監(jiān)督管理局(NMPA)批準(zhǔn)用于轉(zhuǎn)移性結(jié)直腸癌(mCRC)的治療,并被《CSCO結(jié)直腸癌診療指南(2019版)》以zui高等級的1A類證據(jù)、zui大力度的Ⅰ級推薦作為mCRC患者的三線治療標(biāo)準(zhǔn)方案,該推薦等級延續(xù)至今。
隨著研究的不斷深入,呋喹替尼在聯(lián)合用藥方面進(jìn)行了更多探索。在今年的美國臨床腫瘤學(xué)會(ASCO)大會上,同濟(jì)大學(xué)附屬東方醫(yī)院李進(jìn)教授團(tuán)隊發(fā)表了一項研究報告,探索了呋喹替尼聯(lián)合信迪利單抗在晚期結(jié)直腸癌(CRC)治療領(lǐng)域的初步應(yīng)用數(shù)據(jù),將中國實力展現(xiàn)在國際舞臺,推動了我國科研技術(shù)向“國際引領(lǐng)者”邁進(jìn)的步伐。在這個激動人心的時刻,本報特邀李進(jìn)教授分享相關(guān)研究成果,展望抗腫瘤領(lǐng)域的未來前景。
研究速遞

研究名稱
呋喹替尼聯(lián)合信迪利單抗治療晚期CRC的Ib期研究初步結(jié)果
研究背景
本研究的目的是探索呋喹替尼(VEGFR抑制劑)聯(lián)合信迪利單抗(PD-1單抗),治療晚期CRC及其他實體瘤患者的安全性和協(xié)同抗腫瘤效應(yīng)。
研究方法
該研究為Ib期多中心臨床研究,納入了包括CRC在內(nèi)的各類型腫瘤,目前研究仍在進(jìn)行中,本次報告的為mCRC治療組。該治療組共納入44例至少經(jīng)氟尿嘧啶、奧沙利鉑或伊立替康二線治療失敗的mCRC患者,接受呋喹替尼 [5 mg、每日一次、間歇性給藥(連續(xù)服藥2周、停藥1周),或3 mg、每日一次、連續(xù)給藥;每隊n=22] 和信迪利單抗(200 mg,每3周一次)聯(lián)合治療,旨在評估該聯(lián)合方案治療mCRC的安全性和協(xié)同抗腫瘤效應(yīng)。主要研究終點為安全性、耐受性及Ⅱ期臨床研究推薦劑量(RP2D),次要終點為客觀緩解率(ORR)。

研究結(jié)果
截至2021年1月5日,共有44例患者入選,呋喹替尼 [5 mg、每日一次、間歇性給藥(連續(xù)服藥2周、停藥1周)] 聯(lián)合信迪利單抗(200 mg,每3周一次)被確定為RP2D。在44例意向性治療(ITT)人群中,ORR為22.7%,疾病控制率(DCR)為86.4%,中位無進(jìn)展生存期(PFS)為5.6個月,中位總生存期(OS)為11.8個月。在RP2D隊列中,ORR為27.3%,DCR為95.5%,中位PFS為6.9個月。
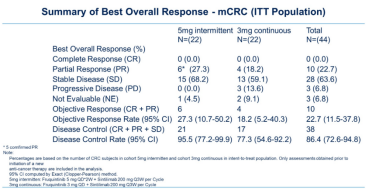
研究結(jié)論
呋喹替尼聯(lián)合信迪利治療用于標(biāo)準(zhǔn)治療失敗或不適合進(jìn)行標(biāo)準(zhǔn)治療的晚期CRC患者,安全可控、耐受性好,且顯示出極具前景的抗腫瘤活性。
呋喹替尼聯(lián)合信迪利單抗研究結(jié)果令人振奮
論壇報:本次ASCO會議上,您和您的團(tuán)隊報告了一項呋喹替尼聯(lián)合信迪利單抗治療晚期CRC的Ib期研究初步結(jié)果,首先想請您分享一下此時此刻您的感受?
李進(jìn)教授:本研究是呋喹替尼聯(lián)合信迪利單抗治療晚期CRC的前瞻性探索研究,得到全國多家中心的大力支持,相關(guān)成果已在本次ASCO會議報道。雖然入組病例不多,但卻獲得了令人振奮的成果。未來也將繼續(xù)探索該聯(lián)合方案在其他消化道腫瘤、肺癌、乳腺癌、肝癌等多種我國高發(fā)的實體腫瘤中的有效性和安全性,期待能夠有更多研究中心參與進(jìn)來,為廣大腫瘤患者帶來福音!
單藥治療效果亮眼聯(lián)合治療再創(chuàng)佳績
論壇報:請問您及您的研究團(tuán)隊此次開展呋喹替尼聯(lián)合信迪利單抗研究的初衷是?呋喹替尼聯(lián)合PD-1單抗治療的優(yōu)勢有哪些?
李進(jìn)教授:基于前期FRESCO研究的結(jié)果,呋喹替尼在2018年9月于我國獲批上市。在臨床實踐過程中發(fā)現(xiàn),無論是臨床試驗或是真實世界研究中,均有諸多證據(jù)表明呋喹替尼可以顯著延長CRC患者三線治療的生存期和疾病控制持續(xù)時間。然而,呋喹替尼單藥為CRC患者帶來的獲益仍較為有限,尚需探索更多聯(lián)合治療策略以更好地幫助患者。
隨著免疫治療時代的到來,免疫檢查點抑制劑在肺癌、肝癌、淋巴瘤等多個瘤種的治療中取得了重大突破,實現(xiàn)了一定程度上的長期生存,將抗腫瘤治療推向了新的高度。基于此,研究者們不斷地進(jìn)行更多聯(lián)合治療方案的探索,以期進(jìn)一步提高免疫治療療效。其中,免疫檢查點抑制劑聯(lián)合小分子靶向藥物的聯(lián)合方案進(jìn)展迅速,但在CRC治療領(lǐng)域卻始終未曾取得令人滿意的成果,有效率不足20%,疾病控制時間也較短。鑒于FRESCO研究取得的亮眼成績,我們開展了呋喹替尼聯(lián)合信迪利單抗治療晚期CRC的臨床研究,進(jìn)一步探索呋喹替尼聯(lián)合免疫治療的抗腫瘤效應(yīng)。
在本次匯報的Ib期研究中,對不同的用藥劑量和給藥間期進(jìn)行了探索,進(jìn)一步確定了呋喹替尼 [5 mg、每日一次、間歇性給藥(連續(xù)服藥2周、停藥1周)] 聯(lián)合信迪利單抗(200 mg,每3周一次)的用藥方案,可實現(xiàn)更佳的安全性和有效性。未來,我們也將采用這一聯(lián)合治療方式開展Ⅱ/Ⅲ期臨床研究,或者針對CRC患者治療的頭對頭研究,如對比目前標(biāo)準(zhǔn)三線治療方案——呋喹替尼單藥與呋喹替尼聯(lián)合信迪利單抗的治療療效,期待為中國乃至全球患者帶來更多切實的幫助。
成為CRC領(lǐng)域里程碑為多瘤種治療奠定基礎(chǔ)
論壇報:請問此次公布的“雙國藥組合”方案,會對我國CRC臨床實踐提供哪些方面的指導(dǎo)和參考?
李進(jìn)教授:所有的臨床研究都需經(jīng)過不斷的探索驗證,再進(jìn)行臨床應(yīng)用。既往中國小分子靶向藥物聯(lián)合PD-1單抗在肝癌治療中已取得重要進(jìn)展,本項I期研究作為國產(chǎn)TKI聯(lián)合PD-1單抗治療CRC患者研究的領(lǐng)跑者,取得了振奮人心的成果,是中國新藥創(chuàng)新進(jìn)步和發(fā)展過程中鼓舞人心的里程碑事件。相信隨著未來研究成果在Ⅱ/Ⅲ期臨床研究中得到進(jìn)一步驗證,將為CRC治療領(lǐng)域帶來重大突破,也為呋喹替尼聯(lián)合信迪利單抗治療其他腫瘤患者打下堅實基礎(chǔ)。期待未來通過不斷的探索和創(chuàng)新,能夠更大化發(fā)揮藥物療效,讓更多患者從治療中獲益,這也是我們作為臨床醫(yī)生和科研工作者的初衷。
助力企業(yè)實現(xiàn)創(chuàng)新轉(zhuǎn)化期待早日實現(xiàn)健康中國
論壇報:可否請您談?wù)劊磥砟湍膱F(tuán)隊還會在哪些方面開展更多學(xué)術(shù)研究?您對于我國本土創(chuàng)新藥物的未來有哪些方面的期待?
李進(jìn)教授:中國原研創(chuàng)新藥物從十余年前起步,到如今已經(jīng)取得了較大的成就。很多產(chǎn)品不僅為國內(nèi)患者帶來幫助,也進(jìn)入了國際醫(yī)藥領(lǐng)域,造福全球患者。毫無疑問,我們在新藥研發(fā)的過程中經(jīng)歷了很多艱辛和困難,慶幸的是在全國民族制藥企業(yè)和廣大臨床專家的不懈堅持和共同努力下,我國原研創(chuàng)新藥物不斷取得了重大突破。
然而,我們目前與西方發(fā)達(dá)國家水平仍有一些差距,我謹(jǐn)代表同濟(jì)大學(xué)附屬東方醫(yī)院臨床研究中心,期盼未來能夠通過不懈努力,為中國藥物創(chuàng)新作出更多貢獻(xiàn)。目前,我們中心有100余項臨床研究正在開展,其中I期研究多達(dá)70余項,期待未來能夠通過I期研究的優(yōu)異數(shù)據(jù),快速幫助制藥企業(yè)提高新產(chǎn)品質(zhì)量標(biāo)準(zhǔn),通過真實可靠的研究數(shù)據(jù),實現(xiàn)從“me-too / me-better”到“源頭創(chuàng)新”的模式轉(zhuǎn)化,并為進(jìn)一步的Ⅱ/Ⅲ期臨床研究提供助力,為藥物創(chuàng)新增添支持力量。相信未來在國家大力的支持和推動下,中國制藥創(chuàng)新將迎來新的高峰,助力推薦健康中國建設(shè)。
來源:腫瘤資訊






